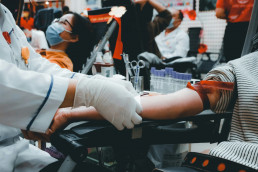
Ежедневно Служба крови направляет большие усилия на заготовку донорской крови. Одной из наиболее важных проблем остается проблема безопасности и качества компонентов донорской крови.
На самых первых этапах перед донацией внимание уделяется обследованию донора. Врач проводит опрос на предмет выявления инфекций. Помимо этого, у донора забирается кровь из вены на ряд анализов, в том числе на гемотрансмиссивные инфекции — ВИЧ, гепатит В и С, сифилис. Полученные результаты позволяют отбраковать кровь доноров, которая может нести в себе риск заражения при ее переливании пациентам.
Однако, технические возможности лабораторного тестирования крови не всегда дают полную гарантию ее вирусобезопасности. Такое может быть в том случае, когда донор уже является вирусоносителем, но количество копий вируса так мало, что тест в момент исследования не может уловить данный вирус, так как прошло незначительное количество времени с периода заражения.
Что делать в таких ситуациях, чтобы обезопасить компоненты крови?
В Службе крови были разработаны и внедрены различные методы по обеспечению безопасности компонентов крови. Один из них – метод карантинизации.
Как правило, «карантину» подвергают свежезамороженную плазму. В течение 180 дней (по новому Постановлению, вышедшему в 2019г. — 120 дней) плазма хранится при температуре ниже -25 С в специальных морозильных камерах. За это время возможно проявление вирусов не в той плазме, которую взяли у донора, а в крови самого донора. После пройденного срока карантинизации и повторного обследования донора крови на гемотрансфмиссивные инфекции, при полученных отрицательных анализах, компонент крови выдают в лечебные учреждения или на переработку на препараты крови. Если у донора выявляют инфекцию или донор просто не явился на повторное исследование, плазму утилизируют. Поэтому повторный приход донора в учреждения Службы крови очень важен!
Метод карантинизации применим и к эритроцитсодержащим компонентам крови — криоконсервирование позволяет сохранять их в течение времени, достаточного для исключения гемотрансмиссивных инфекций. Но на практике данный метод не нашел широкого применения. В основном ограничиваются криоконсервированием и карантинизацией донорских эритроцитов редких групп крови и фенотипов для пополнения банка крови.
В настоящее время для создания безопасности эритроцитсодержащих компонентов крови очень важно, чтобы:
- они заготавливались в специальном растворе, который позволит убрать большую часть плазмы, с которой могут передаваться инфекционные агенты;
- эритроциты подвергались фильтрации как при заготовке компонента крови, так и при переливании непосредственно у постели больного с помощью специальных устройств – фильтров.
Метод отмывания эритроцитов в физиологическом растворе от плазмы, лейкоцитов и тромбоцитов также позволяет повысить безопасность компонентов
Наиболее перспективными методами обеспечения безопасности компонентов крови на сегодняшний день являются технологии инактивации патогенов: вирусов, бактерий, простейших.
Под инактивацией подразумевается группа методов, позволяющих инактивировать (уничтожить) гемотрансмиссивные инфекции, вызванные патогенами в компонентах донорской крови и препаратах, что позволяет выполнять в последующем переливание крови пациентам и применять препараты крови без риска инфицирования.
 Рисунок 1, 2 – Аппарат «INTERCEPT». Подготовка аппарата и тромбоцитов к вирусинактивации.
Рисунок 1, 2 – Аппарат «INTERCEPT». Подготовка аппарата и тромбоцитов к вирусинактивации.
На практике чаще всего используется вирусинактивация плазмы и тромбоцитов.
Для процедуры вирусинактивации необходимо специальное оборудование, которое позволяет быстро и качественно заготовить безопасный компонент. Так, например, для инактивации плазмы используется аппарат «Макотроник», который облучает видимым светом плазму около 20 минут после добавления к ней специального красителя – метиленовой сини. Суть заключается в том, что краситель способен внедряться в структуру вируса. После облучения светом образуется кислород с высокой энергией, который повреждает генетический материал вируса.
Инактивация тромбоцитов проходит в аппарате «INTERCEPT». В нем может происходить и инактивация патогенов плазмы (рис. 1, 2). Метод основан на применении фотоактивного вещества амотосолена, мишенями которого является также генетический материал патогенов. При добавлении амотосолена в плазму или тромбоконцентрат и последующем ультрафиолетовым облучением происходит фотохимическая реакция вещества с материалом вирусов, бактерий, простейших. В результате все патогены инактивируются и компонент крови становится безопасным для пациента.
Существуют и другие системы и методы по инактивации патогенов, принцип создания безопасности которых примерно одинаков с приведенными.
Актуальность данной проблемы остается важной и по сей день. Медицина развивается стремительными шагами, и в области Службы крови есть большие продвижения. Новые знания и исследования позволяют применять на практике различные технологии для повышения качества и безопасности выпускаемых компонентов крови. Ведь безопасность компонентов крови – главный принцип, которого необходимо придерживаться 24 часа в сутки 7 дней в неделю при переливании компонентов крови пациентам.
Хафизова Екатерина Эдуардовна
Врач-трансфузиолог ГАУЗ «РЦК МЗ РТ»
Стань донором крови!
Сдавать кровь — простой способ спасать жизни людей. Становитесь донором и регистрируйтесь в DonorSearch, чтобы следить за своими донациями и получать приятные бонусы!